انتقال شیشه به مایع یا انتقال شیشه ای ، انتقال تدریجی و برگشت پذیر در مواد بی شکل (یا در مناطق بی شکل در مواد نیمه بلوری ) از حالت شیشه ای سخت و نسبتا شکننده به حالت چسبناک یا لاستیکی با افزایش دما است. جامد آمورف که انتقال شیشه ای را نشان می دهد شیشه نامیده می شود . انتقال معکوس که با فوق خنک کردن مایع چسبناک به حالت شیشه ای حاصل می شود، انجماد نامیده می شود .
دمای انتقال شیشهای Tg یک ماده، محدوده دماهایی را که این انتقال شیشهای روی آن اتفاق میافتد را مشخص میکند (به عنوان یک تعریف تجربی، که معمولاً به عنوان 100 ثانیه زمان آرامش مشخص میشود) . در صورت وجود ، همیشه کمتر از دمای ذوب ، Tm ، حالت کریستالی ماده است.
پلاستیک های سخت مانند پلی استایرن و پلی (متیل متاکریلات) بسیار کمتر از دمای انتقال شیشه ای خود استفاده می شوند، یعنی زمانی که در حالت شیشه ای خود هستند. مقادیر Tg آنها هر دو در حدود 100 درجه سانتیگراد (212 درجه فارنهایت) است . الاستومرهای لاستیکی مانند پلی ایزوپرن و پلی ایزوبوتیلن بالاتر از Tg خود استفاده می شوند ، یعنی در حالت لاستیکی، جایی که نرم و انعطاف پذیر هستند. اتصال عرضی از جریان آزاد مولکولهای آنها جلوگیری میکند، بنابراین به لاستیک یک شکل تنظیم شده در دمای اتاق (بر خلاف مایع چسبناک) میدهد. [3]
علیرغم تغییر در خواص فیزیکی یک ماده از طریق انتقال شیشه ای آن، این انتقال یک انتقال فاز در نظر گرفته نمی شود . بلکه پدیده ای است که در یک محدوده دما گسترش می یابد و توسط یکی از چندین قرارداد تعریف می شود. [2] [4] [5] چنین قراردادهایی شامل نرخ خنکسازی ثابت (20 کلوین در دقیقه (36 درجه فارنهایت در دقیقه)) [1] و آستانه ویسکوزیته 1012 Pa ·s و غیره است. به محض سرد شدن یا گرم شدن در این محدوده انتقال شیشه ای، ماده همچنین یک مرحله صاف در ضریب انبساط حرارتی و در گرمای ویژه نشان می دهد که مکان این اثرات دوباره به تاریخچه مواد بستگی دارد. [6] این سوال که آیا برخی از انتقال فاز زمینه ساز انتقال شیشه ای است یا خیر، موضوع تحقیقات در حال انجام است.
انتقال شیشه ای (در علم پلیمر): فرآیندی که در آن مذاب پلیمری با سرد شدن به شیشه پلیمری یا شیشه پلیمری با حرارت دادن به مذاب پلیمری تغییر می کند. [8]
- پدیدههایی که در انتقال شیشهای پلیمرها رخ میدهند هنوز در معرض تحقیقات و بحثهای علمی مداوم هستند. انتقال شیشه ای ویژگی های یک انتقال مرتبه دوم را نشان می دهد زیرا مطالعات حرارتی اغلب نشان می دهد که انرژی های گیبس مولی، آنتالپی های مولی و حجم های مولی دو فاز، یعنی مذاب و شیشه، برابر هستند، در حالی که ظرفیت گرمایی و انبساط ناپیوسته است. با این حال، با توجه به مشکل ذاتی در رسیدن به تعادل در یک شیشه پلیمری یا در یک مذاب پلیمری در دماهای نزدیک به دمای انتقال شیشه، انتقال شیشه ای به طور کلی به عنوان یک انتقال ترمودینامیکی در نظر گرفته نمی شود.
- در مورد پلیمرها، تغییرات ساختاری بخشها، که معمولاً از 10 تا 20 اتم زنجیره اصلی تشکیل شدهاند، در زیر دمای انتقال شیشهای بینهایت کند میشوند.
- در یک پلیمر تا حدی کریستالی، انتقال شیشه تنها در قسمتهای آمورف ماده رخ میدهد.
- این تعریف با آنچه در ref. [9]
- اصطلاح رایج “گذر شیشه ای به لاستیک” برای انتقال شیشه ای توصیه نمی شود. [8]
خصوصیات
انتقال شیشه ای مایع به حالت جامد مانند ممکن است با خنک کردن یا فشرده سازی رخ دهد. [10] این انتقال شامل افزایش هموار ویسکوزیته یک ماده به میزان 17 مرتبه قدر در محدوده دمایی 500 کلوین است بدون اینکه هیچ تغییری در ساختار ماده ایجاد شود. [2] [11] این انتقال برخلاف انتقال انجماد یا تبلور است که یک انتقال فاز مرتبه اول در طبقهبندی Ehrenfest است و شامل ناپیوستگیهایی در خواص ترمودینامیکی و دینامیکی مانند حجم، انرژی و ویسکوزیته است. در بسیاری از موادی که معمولاً تحت یک انتقال انجماد قرار میگیرند، خنکسازی سریع از این انتقال فاز جلوگیری میکند و در عوض منجر به انتقال شیشهای در دمای پایینتر میشود. مواد دیگر، مانند بسیاری از پلیمرها ، فاقد حالت کریستالی مشخص هستند و به راحتی شیشه ها را تشکیل می دهند، حتی در صورت خنک شدن یا فشرده سازی بسیار آهسته. به تمایل مواد برای تشکیل شیشه در هنگام خاموش شدن، توانایی تشکیل شیشه می گویند. این توانایی به ترکیب مواد بستگی دارد و با تئوری صلبیت قابل پیش بینی است . [12]
در زیر محدوده دمای انتقال، ساختار شیشه ای مطابق با نرخ خنک کننده استفاده شده شل نمی شود. ضریب انبساط برای حالت شیشه ای تقریباً معادل ضریب انبساط جامد کریستالی است. اگر از سرعت خنکسازی کندتر استفاده شود، افزایش زمان برای آرامش ساختاری (یا بازآرایی بین مولکولی) ممکن است منجر به یک محصول شیشهای با چگالی بالاتر شود. به طور مشابه، با بازپخت (و در نتیجه ایجاد آرامش ساختاری آهسته) ساختار شیشه در زمان به چگالی تعادلی مربوط به مایع فوق سرد در همین دما نزدیک می شود. Tg در تقاطع بین منحنی خنک کننده (حجم در مقابل دما) برای حالت شیشه ای و مایع فوق خنک قرار دارد . [2] [13] [14] [15] [16] [17]
پیکربندی شیشه در این محدوده دما به آرامی با زمان به سمت ساختار تعادل تغییر می کند. اصل به حداقل رساندن انرژی آزاد گیبس نیروی محرکه ترمودینامیکی لازم برای تغییر نهایی را فراهم می کند. در دماهای تا حدودی بالاتر از Tg ، ساختار مربوط به تعادل در هر دما بسیار سریع به دست می آید. در مقابل، در دماهای به طور قابل توجهی پایین تر، پیکربندی شیشه در طول دوره های زمانی به طور فزاینده ای پایدار باقی می ماند.
بنابراین، انتقال شیشه مایع یک انتقال بین حالتهای تعادل ترمودینامیکی نیست . باور عمومی بر این است که حالت تعادل واقعی همیشه کریستالی است. اعتقاد بر این است که شیشه در یک حالت قفل جنبشی وجود دارد و آنتروپی، چگالی و غیره آن به تاریخچه حرارتی بستگی دارد. بنابراین، انتقال شیشه ای در درجه اول یک پدیده پویا است. زمان و دما مقادیر قابل تعویض (تا حدی) هنگام برخورد با شیشه ها هستند، این واقعیت اغلب در اصل برهم نهی دما-زمان بیان می شود . با خنک کردن مایع، درجات آزادی داخلی متوالی از حالت تعادل خارج میشوند . با این حال، یک بحث طولانی مدت وجود دارد که آیا یک انتقال مرحله مرتبه دوم اساسی در حد فرضی زمانهای آرامش بینهایت طولانی وجود دارد. [ توضیحات لازم ] [6] [19] [20] [21]
در یک مدل جدیدتر انتقال شیشه ای، دمای انتقال شیشه ای مربوط به دمایی است که در آن بزرگ ترین منافذ بین عناصر ارتعاشی در ماتریس مایع کوچکتر از کوچکترین سطح مقطع عناصر یا قسمت هایی از آنها در هنگام کاهش دما می شود. . در نتیجه نوسان ورودی انرژی حرارتی به ماتریس مایع، هارمونیک نوسانات دائماً مختل می شود و حفره های موقتی (“حجم آزاد”) بین عناصر ایجاد می شود که تعداد و اندازه آنها به دما بستگی دارد. دمای انتقال شیشه ای Tg0 که در این روش تعریف شده است، یک ثابت ماده ثابت در حالت بی نظم (غیر بلوری) است که فقط به فشار وابسته است. در نتیجه افزایش اینرسی ماتریس مولکولی هنگام نزدیک شدن به Tg0 ، تنظیم تعادل حرارتی به طور متوالی به تأخیر می افتد، به طوری که روش های اندازه گیری معمول برای تعیین دمای انتقال شیشه ای در اصل مقادیر Tg بسیار بالا را ارائه می دهند. در اصل، هرچه سرعت تغییر دما در طول اندازهگیری کندتر تنظیم شود، به مقدار Tg اندازهگیری شده Tg0 نزدیکتر میشود. [22] تکنیک هایی مانند تحلیل مکانیکی دینامیکی را می توان برای اندازه گیری دمای انتقال شیشه ای استفاده کرد.
![]()
دمای انتقال Tg
|
|
این بخش به نقل قول های اضافی برای تأیید نیاز دارد . ( جولای 2009 )
|


به شکل پایین سمت راست که ظرفیت گرمایی را به عنوان تابعی از دما ترسیم می کند، مراجعه کنید. در این زمینه، Tg دمای مربوط به نقطه A در منحنی است. [24]
تعاریف عملیاتی متفاوتی از دمای انتقال شیشه ای Tg در حال استفاده است و تعدادی از آنها به عنوان استانداردهای علمی پذیرفته شده تایید شده اند. با این وجود، همه تعاریف دلخواه هستند و همگی نتایج عددی متفاوتی را به دست میدهند: در بهترین حالت، مقادیر Tg برای یک ماده معین در چند کلوین مطابقت دارند. یک تعریف به ویسکوزیته اشاره دارد که Tg را در مقدار 10 13 پویز (یا 10 12 Pa·s) ثابت می کند . همانطور که به طور تجربی نشان داده شد، این مقدار نزدیک به نقطه بازپخت بسیاری از شیشه ها است. [25]
برخلاف ویسکوزیته، انبساط حرارتی ، ظرفیت حرارتی ، مدول برشی و بسیاری از خواص دیگر شیشه های معدنی تغییر نسبتاً ناگهانی در دمای انتقال شیشه ای نشان می دهد. از هر گام یا پیچیدگی می توان برای تعریف Tg استفاده کرد . برای اینکه این تعریف قابل تکرار باشد، باید میزان سرمایش یا گرمایش مشخص شود.
متداول ترین تعریف Tg از آزاد شدن انرژی در گرمایش در کالریمتری اسکن تفاضلی استفاده می کند (DSC، شکل را ببینید). به طور معمول، نمونه ابتدا با 10 K/min خنک می شود و سپس با همان سرعت گرم می شود.
تعریف دیگری از Tg از پیچ خوردگی در دیلاتومتری (معروف به انبساط حرارتی) استفاده می کند: به شکل بالا سمت راست مراجعه کنید. در اینجا، نرخ گرمایش 3-5 K/min (5.4-9.0 درجه فارنهایت در دقیقه) رایج است. مقاطع خطی زیر و بالای Tg به رنگ سبز هستند . Tg درجه حرارت در تقاطع خطوط رگرسیون قرمز است . [24]
در زیر مقادیر Tg مشخصه کلاس های خاصی از مواد خلاصه شده است .
پلیمرها [ ویرایش ]
| مواد | Tg ( درجه سانتیگراد) | Tg ( درجه فارنهایت) | نام تجاری |
|---|---|---|---|
| لاستیک تایر | -70 | −94 [26] | |
| پلی وینیلیدین فلوراید (PVDF) | -35 | −31 [27] | |
| پلی پروپیلن (PP atactic) | -20 | -4 [28] | |
| پلی وینیل فلوراید (PVF) | -20 | -4 [27] | |
| پلی پروپیلن (PP ایزوتاکتیک) | 0 | 32 [28] | |
| پلی 3 هیدروکسی بوتیرات (PHB) | 15 | 59 [28] | |
| پلی (وینیل استات) (PVAc) | 30 | 86 [28] | |
| پلی کلروتری فلوئورواتیلن (PCTFE) | 45 | 113 [27] | |
| پلی آمید (PA) | 47-60 | 117-140 | نایلون-6، x |
| پلی لاکتیک اسید (PLA) | 60-65 | 140-149 | |
| پلی اتیلن ترفتالات (PET) | 70 | 158 [28] | |
| پلی (وینیل کلراید) (PVC) | 80 | 176 [28] | |
| پلی (وینیل الکل) (PVA) | 85 | 185 [28] | |
| پلی استایرن (PS) | 95 | 203 [28] | |
| پلی (متیل متاکریلات) (PMMA atactic) | 105 | 221 [28] | پلکسی گلاس، پرسپکس |
| اکریلونیتریل بوتادین استایرن (ABS) | 105 | 221 [29] | |
| پلی تترا فلوئورواتیلن (PTFE) | 115 | 239 [30] | تفلون |
| پلی (کربنات) (کامپیوتر) | 145 | 293 [28] | لکسان |
| پلی سولفون | 185 | 365 | |
| پلی نوربورن | 215 | 419 [28] |
نایلون خشک 6 دمای انتقال شیشه ای 47 درجه سانتیگراد (117 درجه فارنهایت) دارد. [31] نایلون-6،6 در حالت خشک دمای انتقال شیشه ای در حدود 70 درجه سانتیگراد (158 درجه فارنهایت) دارد. [32] [33] در حالی که پلی اتن دارای محدوده انتقال شیشه ای 130- تا 80- درجه سانتی گراد (202- تا 112- درجه فارنهایت) است [34] موارد فوق فقط مقادیر متوسط هستند، زیرا دمای انتقال شیشه به سرعت خنک شدن بستگی دارد. و توزیع وزن مولکولی و می تواند تحت تأثیر مواد افزودنی قرار گیرد. برای یک ماده نیمه کریستالی، مانند پلی اتنی که در دمای اتاق 60 تا 80 درصد کریستالی است، انتقال شیشه ای نقل شده به اتفاقی که برای بخش آمورف ماده پس از سرد شدن می افتد اشاره دارد.
سیلیکات ها و سایر شیشه های شبکه کووالانسی [ ویرایش ]
| مواد | Tg ( درجه سانتیگراد) | Tg ( درجه فارنهایت) |
|---|---|---|
| کالکوژنید GeSbTe | 150 | 302 [35] |
| کالکوژنید AsGeSeTe | 245 | 473 |
| شیشه فلوراید ZBLAN | 235 | 455 |
| دی اکسید تلوریوم | 280 | 536 |
| فلوروآلومینات | 400 | 752 |
| لیوان سودا آهک | 520–600 | 968-1112 |
| کوارتز ذوب شده (تقریبی) | 1200 | 2200 [36] |
پارادوکس کائوزمن [ ویرایش ]

هنگامی که یک مایع فوق سرد می شود، تفاوت آنتروپی بین فاز مایع و جامد کاهش می یابد. با برون یابی ظرفیت حرارتی مایع فوق سرد شده به زیر دمای انتقال شیشه ای آن ، می توان دمایی را محاسبه کرد که در آن اختلاف آنتروپی ها صفر می شود. این دما دمای کائوزمن نامیده شده است . [2]
اگر مایعی بتواند زیر دمای کائوزمن خود فوق سرد شود و در واقع آنتروپی کمتری نسبت به فاز بلوری نشان دهد، عواقب آن متناقض خواهد بود. این پارادوکس کاوزمن از زمانی که برای اولین بار توسط والتر کاوزمن در سال 1948 مطرح شد، موضوع بحث های زیادی و انتشارات بسیاری بوده است. [37] [38]
یکی از راه حل های پارادوکس کاوزمن این است که بگوییم قبل از کاهش آنتروپی مایع باید یک انتقال فاز وجود داشته باشد. در این سناریو، دمای انتقال به عنوان دمای انتقال شیشه ای ایده آل کالریمتری T 0c شناخته می شود . در این دیدگاه، انتقال شیشه ای صرفاً یک اثر جنبشی نیست ، یعنی صرفاً نتیجه سرد شدن سریع مذاب است، بلکه یک مبنای ترمودینامیکی زیربنایی برای تشکیل شیشه وجود دارد. دمای انتقال شیشه ای:
- تی�→تی0ج مانند دتیدتی→0.
مدل Gibbs-DiMarzio از سال 1958 [39] به طور خاص پیش بینی می کند که آنتروپی پیکربندی مایع فوق سرد شده در حد ناپدید می شود.تی→تیک+، جایی که رژیم وجود مایع به پایان می رسد، ریزساختار آن با کریستال یکسان می شود و منحنی های ویژگی آنها در یک انتقال فاز مرتبه دوم واقعی قطع می شود. این هرگز بهدلیل دشواری درک نرخ خنککننده به اندازه کافی آهسته و در عین حال اجتناب از کریستالیزاسیون تصادفی، بهطور تجربی تأیید نشده است. مدل آدام-گیبز در سال 1965 [40] تفکیک پارادوکس کاوزمن را پیشنهاد کرد که بر اساس آن زمان آرامش در دمای کاوزمن متفاوت است، به این معنی که هرگز نمیتوان مایع فوقپایدار فوقسرد شده را در اینجا متعادل کرد. یک بحث انتقادی در مورد پارادوکس کاوزمن و مدل آدام-گیبز در سال 2009 ارائه شد. [41] داده های چند مایع آلی فوق خنک پیش بینی آدام-گیبز از زمان استراحت واگرا در هر دمای محدود، به عنوان مثال دمای کاوزمن را تایید نمی کند. [42]
قطعنامه های جایگزین [ ویرایش ]
حداقل سه راه حل ممکن دیگر برای پارادوکس کاوزمن وجود دارد. ممکن است ظرفیت گرمایی مایع فوق خنک در نزدیکی دمای کاوزمن به آرامی به مقدار کمتری کاهش یابد. همچنین ممکن است یک انتقال مرحله اول به حالت مایع دیگر قبل از دمای کاوزمن اتفاق بیفتد که ظرفیت گرمایی این حالت جدید کمتر از آن است که با برون یابی از دمای بالاتر به دست می آید. در نهایت، کائوزمن خود پارادوکس آنتروپی را با این فرض حل کرد که تمام مایعات فوق سرد باید قبل از رسیدن به دمای کائوزمن متبلور شوند.
در مواد خاص [ ویرایش ]
سیلیس، SiO 2 [ ویرایش ]
سیلیس (ترکیب شیمیایی SiO 2 ) علاوه بر ساختار کوارتز، دارای تعدادی اشکال کریستالی متمایز است. تقریباً تمام اشکال کریستالی شامل واحدهای SiO 4 چهار وجهی است که توسط رئوس مشترک در آرایشهای مختلف به هم مرتبط شدهاند ( stishovite ، متشکل از هشتوجهی SiO 6 متصل ، استثنای اصلی است). طول پیوند Si-O بین اشکال کریستالی مختلف متفاوت است. برای مثال، در کوارتز α، طول پیوند 161 پیکومتر (6.3 × 10-9 اینچ) است، در حالی که در α-تریدیمیت از 154 تا 171 pm (6.1 × 10-9 -6.7 × 10-9 اینچ ) متغیر است . زاویه پیوند Si-O-Si نیز از 140 درجه در α-تریدیمیت تا 144 درجه در α-کوارتز تا 180 درجه در β-تریدیمیت متغیر است. هر گونه انحراف از این پارامترهای استاندارد، تفاوتها یا تغییرات ریزساختاری را ایجاد میکند که نشاندهنده رویکردی به جامدات آمورف ، زجاجیه یا شیشهای است . دمای انتقال Tg در سیلیکات ها مربوط به انرژی مورد نیاز برای شکستن و تشکیل مجدد پیوندهای کووالانسی در شبکه آمورف (یا شبکه تصادفی) از پیوندهای کووالانسی است . Tg به وضوح تحت تأثیر شیمی شیشه است . به عنوان مثال، افزودن عناصری مانند B ، Na ، K یا Ca به یک لیوان سیلیسی که ظرفیت آنها کمتر از 4 است، به شکستن ساختار شبکه و در نتیجه کاهش Tg کمک می کند . از طرف دیگر، P که ظرفیت آن 5 است، به تقویت یک شبکه منظم کمک می کند و بنابراین Tg را افزایش می دهد . [43] Tg مستقیماً با استحکام پیوند متناسب است، به عنوان مثال به پارامترهای ترمودینامیکی شبه تعادلی پیوندها بستگی دارد به عنوان مثال بر روی آنتالپی Hd و آنتروپی Sd پیکربندی – پیوندهای شکسته : Tg = Hd / [ S d + Rln[(1- fc ) / fc ] که در آن R ثابت گاز و fc آستانه نفوذ است. برای مذاب های قوی مانند Si O 2 آستانه نفوذ در معادله فوق چگالی بحرانی جهانی Scher-Zallen در فضای سه بعدی است به عنوان مثال f c 0.15 =، اما برای مواد شکننده، آستانه نفوذ به مواد وابسته است و fc ≪ 1 است . [45]
پلیمرها [ ویرایش ]
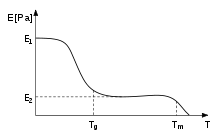
در پلیمرها ، دمای انتقال شیشهای، Tg ، اغلب به صورت دمایی بیان میشود که در آن انرژی آزاد گیبس به گونهای است که انرژی فعالسازی برای حرکت مشارکتی 50 یا بیشتر عنصر پلیمر از آن فراتر رود [ نیازمند منبع ] . این به زنجیره های مولکولی اجازه می دهد تا با اعمال نیرو از کنار یکدیگر بگذرند. از این تعریف، میتوان دریافت که معرفی گروههای شیمیایی نسبتاً سفت (مانند حلقههای بنزن ) در فرآیند جاری شدن اختلال ایجاد میکند و در نتیجه Tg را افزایش میدهد . [46] سفتی ترموپلاستیک ها به دلیل این اثر کاهش می یابد (شکل را ببینید.) هنگامی که دمای شیشه به دست آمد، سفتی برای مدتی ثابت می ماند، یعنی در E 2 یا نزدیک به آن، تا زمانی که دما از Tm تجاوز کند ، و مواد ذوب می شود این منطقه فلات لاستیکی نامیده می شود.

مدول برشی که از سمت دمای پایین می آید، در دمای انتقال شیشه ای Tg به مراتب افت می کند . یک رابطه ریاضی در سطح مولکولی برای مدول برشی وابسته به دما شیشه پلیمری در نزدیک شدن به Tg از پایین توسط Alessio Zaccone و Eugene Terentjev ایجاد شده است . [47] حتی اگر مدول برشی واقعاً به صفر نمیرسد (به مقدار بسیار پایینتر فلات لاستیکی کاهش مییابد)، با صفر کردن مدول برشی در فرمول Zaccone-Terentjev، عبارتی برای Tg به دست میآید. که معادله فلوری-فاکس را بازیابی می کند و همچنین نشان می دهد که Tg با ضریب انبساط حرارتی در حالت شیشه ای نسبت معکوس دارد . این روش پروتکل عملیاتی دیگری را برای تعریف Tg شیشه های پلیمری با شناسایی آن با دمایی که در آن مدول برشی با مرتبه های بزرگی به سطح فلات لاستیکی کاهش می یابد، ارائه می دهد.
در اتو کردن ، پارچه ای از طریق این انتقال گرم می شود تا زنجیره های پلیمری متحرک شوند. سپس وزن آهن جهت گیری ترجیحی را تحمیل می کند. Tg را می توان با افزودن نرم کننده ها به ماتریس پلیمری به طور قابل توجهی کاهش داد. مولکولهای کوچکتر نرمکننده خود را بین زنجیرههای پلیمری قرار میدهند، فاصله و حجم آزاد را افزایش میدهند و به آنها اجازه میدهند حتی در دماهای پایینتر از کنار یکدیگر حرکت کنند. افزودن نرمکننده میتواند به طور موثری بر دینامیک زنجیره پلیمری کنترل داشته باشد و بر مقادیر حجم آزاد مرتبط تسلط داشته باشد، به طوری که افزایش تحرک انتهای پلیمری آشکار نباشد. [48] افزودن گروههای جانبی غیرواکنشکننده به یک پلیمر همچنین میتواند زنجیرهها را از یکدیگر جدا کند و Tg را کاهش دهد . اگر پلاستیکی با برخی خواص مطلوب دارای Tg بسیار بالا باشد، گاهی اوقات می توان آن را با دیگری در یک کوپلیمر یا ماده مرکب با Tg کمتر از دمای مورد استفاده ترکیب کرد. توجه داشته باشید که برخی از پلاستیک ها در دماهای بالا، به عنوان مثال، در موتورهای خودرو، و برخی دیگر در دماهای پایین استفاده می شوند. [28]
در مواد ویسکوالاستیک ، وجود رفتار مایع مانند به خواص آن بستگی دارد و بنابراین با نرخ بار اعمال شده، یعنی سرعت اعمال نیرو، متفاوت است. اسباببازی سیلیکونی Silly Putty بسته به سرعت زمان اعمال نیرو کاملاً متفاوت عمل میکند: به آرامی بکشید و جریان پیدا میکند و مانند یک مایع بسیار چسبناک عمل میکند . با چکش به آن ضربه بزنید و خرد می شود و مانند یک لیوان عمل می کند.
در هنگام خنک شدن، لاستیک تحت یک انتقال شیشه مایع قرار می گیرد که به آن انتقال لاستیک به شیشه نیز گفته می شود .
مکانیک انجماد شیشه ای
حرکت مولکولی در ماده متراکم را می توان با یک سری فوریه نشان داد که تفسیر فیزیکی آن شامل برهم نهی امواج طولی و عرضی جابجایی اتمی با جهت ها و طول موج های متفاوت است. در سیستم های تک اتمی به این امواج نوسانات چگالی می گویند . (در سیستم های چند اتمی، آنها همچنین ممکن است شامل نوسانات ترکیبی باشند.) [49]
بنابراین، حرکت حرارتی در مایعات را می توان به ارتعاشات طولی ابتدایی (یا فونون های صوتی ) تجزیه کرد ، در حالی که ارتعاشات عرضی (یا امواج برشی) در اصل فقط در جامدات الاستیک توصیف می شدند که حالت کریستالی بسیار مرتب ماده را نشان می دادند. به عبارت دیگر، مایعات ساده نمی توانند نیروی اعمال شده را به شکل تنش برشی تحمل کنند و به صورت مکانیکی از طریق تغییر شکل پلاستیک ماکروسکوپی (یا جریان چسبناک) تسلیم می شوند. علاوه بر این، این واقعیت که یک جامد در حالی که سفتی خود را حفظ میکند به صورت موضعی تغییر شکل میدهد – در حالی که یک مایع در پاسخ به اعمال نیروی برشی اعمالشده به جریان چسبناک ماکروسکوپی تسلیم میشود – توسط بسیاری به عنوان تمایز مکانیکی بین این دو پذیرفته شده است. [50] [51]
با این حال، فرنکل در تجدید نظر خود در نظریه جنبشی جامدات و نظریه کشش در مایعات به نارسایی های این نتیجه اشاره کرد . این بازبینی مستقیماً از مشخصه پیوسته متقاطع ویسکوالاستیک از حالت مایع به حالت جامد ناشی میشود، زمانی که انتقال با تبلور همراه نباشد – بنابراین مایع چسبناک فوقخنک شده است . بنابراین ما همبستگی نزدیک بین فونون های صوتی عرضی (یا امواج برشی) و شروع صلبیت پس از انجماد را می بینیم ، همانطور که بارتنف در توصیف مکانیکی خود از فرآیند انجماد توضیح داده است. [52] [53] این مفهوم منجر به تعریف انتقال شیشه ای بر حسب ناپدید شدن یا کاهش قابل توجه مدول برشی فرکانس پایین می شود، همانطور که به صورت کمی در کار Zaccone و Terentjev [47] در مثال شیشه پلیمری نشان داده شده است. در واقع، مدل هل دادن تصریح میکند که انرژی فعالسازی زمان آرامش متناسب با مدول برشی فلات فرکانس بالا است، [2] [54] کمیتی که با سرد شدن افزایش مییابد و بنابراین وابستگی دمایی غیر آرنیوسی فراگیر آرامش را توضیح میدهد. زمان در مایعات شیشه ساز
سرعت فونون های آکوستیک طولی در ماده متراکم مستقیماً مسئول هدایت حرارتی است که اختلاف دما بین عناصر حجم فشرده و منبسط شده را کاهش می دهد . کیتل پیشنهاد کرد که رفتار عینک ها بر حسب یک « مسیر آزاد متوسط » تقریباً ثابت برای فونون های شبکه تفسیر می شود و مقدار میانگین مسیر آزاد از مرتبه بزرگی مقیاس بی نظمی در ساختار مولکولی یک است. مایع یا جامد فونون حرارتی میانگین مسیرهای آزاد یا طول آرامش تعدادی از شکلدهندههای شیشه در مقابل دمای انتقال شیشه ترسیم شده است که نشاندهنده رابطه خطی بین این دو است. این یک معیار جدید برای تشکیل شیشه بر اساس مقدار مسیر آزاد میانگین فونون پیشنهاد کرده است. [55]
اغلب پیشنهاد شده است که انتقال گرما در جامدات دی الکتریک از طریق ارتعاشات الاستیک شبکه رخ می دهد، و این انتقال توسط پراکندگی الاستیک فونون های صوتی توسط نقص شبکه محدود می شود (مثلاً فضاهای خالی با فاصله تصادفی). [56] این پیشبینیها با آزمایشهایی بر روی شیشههای تجاری و سرامیکهای شیشهای تأیید شد ، جایی که میانگین مسیرهای آزاد ظاهراً با «پراکندگی مرز داخلی» به مقیاسهای طولی 10-10 میکرومتر (0.00039-0.00394 اینچ) محدود شد. [57] [58] رابطه بین این امواج عرضی و مکانیسم انجماد شیشه ای توسط چندین نویسنده توصیف شده است که پیشنهاد کردند که شروع همبستگی بین این فونون ها منجر به نظم جهت گیری یا “انجماد” تنش های برشی محلی در شکل دهی شیشه می شود. مایعات، بنابراین انتقال شیشه ای ایجاد می شود. [59]
ساختار الکترونیکی [ ویرایش ]
تأثیر فونون های حرارتی و تعامل آنها با ساختار الکترونیکی موضوعی است که در بحث مقاومت فلزات مایع به درستی مطرح شد. نظریه ذوب لیندمن ارجاع شده است، [60] و پیشنهاد می شود که کاهش رسانایی در رفتن از حالت کریستالی به حالت مایع به دلیل افزایش پراکندگی الکترون های رسانایی در نتیجه افزایش دامنه ارتعاش اتمی است . چنین تئوریهای محلیسازی برای انتقال در شیشههای فلزی ، جایی که میانگین مسیر آزاد الکترونها بسیار کوچک است (به ترتیب فاصله بین اتمی) استفاده شده است . [61] [62]
تشکیل یک شکل غیر کریستالی از یک آلیاژ طلا-سیلیکون با استفاده از روش خنثی کردن اسپلیت از مذاب منجر به ملاحظات بیشتر در مورد تأثیر ساختار الکترونیکی بر توانایی شکلدهی شیشه، بر اساس ویژگیهای پیوند فلزی شد . [63] [64] [65] [66] [67]
کار دیگر نشان میدهد که تحرک الکترونهای موضعی با حضور حالتهای فونون پویا افزایش مییابد. یک ادعا علیه چنین مدلی این است که اگر پیوندهای شیمیایی مهم هستند، مدلهای تقریباً الکترون آزاد نباید قابل اجرا باشند. با این حال، اگر مدل شامل ایجاد توزیع بار بین همه جفتهای اتم درست مانند یک پیوند شیمیایی باشد (به عنوان مثال، سیلیکون، زمانی که یک نوار فقط با الکترون پر شده است) باید برای جامدات اعمال شود . [68]
بنابراین، اگر هدایت الکتریکی کم باشد، میانگین مسیر آزاد الکترون ها بسیار کوتاه است. الکترونها فقط به ترتیب برد کوتاه در شیشه حساس خواهند بود زیرا فرصتی برای پراکندگی از اتمهایی که در فواصل زیاد فاصله دارند را ندارند. از آنجایی که ترتیب برد کوتاه در شیشه ها و کریستال ها مشابه است، انرژی های الکترونیکی باید در این دو حالت مشابه باشند. برای آلیاژهایی با مقاومت کمتر و مسیرهای آزاد متوسط الکترونیکی طولانیتر، الکترونها میتوانند شروع به درک [ مشکوک ] کنند که در شیشه بینظمی وجود دارد ، و این باعث افزایش انرژی آنها و بیثبات شدن شیشه نسبت به تبلور میشود. بنابراین، تمایلات تشکیل شیشه آلیاژهای خاص ممکن است تا حدی به این دلیل باشد که مسیرهای آزاد میانگین الکترون بسیار کوتاه هستند، به طوری که فقط ترتیب برد کوتاه برای انرژی الکترون ها مهم است.
همچنین استدلال شده است که تشکیل شیشه در سیستم های فلزی به “نرم” پتانسیل برهمکنش بین اتم ها برخلاف اتم ها مرتبط است. برخی از نویسندگان، با تاکید بر شباهت های قوی بین ساختار محلی شیشه و کریستال مربوطه، پیشنهاد می کنند که پیوند شیمیایی به تثبیت ساختار بی شکل کمک می کند. [69] [70]
سایر نویسندگان پیشنهاد کرده اند که ساختار الکترونیکی تأثیر خود را بر تشکیل شیشه از طریق خواص جهتی پیوندها ایجاد می کند. بنابراین عدم بلورینگی در عناصر با تعداد زیادی اشکال چندشکل و درجه بالایی از ناهمسانگردی پیوند مورد علاقه است . با افزایش ناهمسانگردی پیوند از پیوند فلزی همسانگرد به پیوند فلزی ناهمسانگرد به کووالانسی ، متبلور شدن بعیدتر می شود ، بنابراین ارتباط بین تعداد گروه در جدول تناوبی و توانایی تشکیل شیشه در جامدات عنصری را نشان می دهد . [71]


دیدگاهتان را بنویسید